گاز گلخانه ای دی اکسید کربن را می توان با الکترولیز به هیدروکربن مفید تبدیل کرد، سلول الکترولیز در این فرآیند بسیار مهم است، سلول موسوم به شکاف صفر به ویژه برای فرآیندهای صنعتی مناسب است، اما هنوز مشکلاتی وجود دارد: کاتدها به سرعت مسدود می شوند.
احتراق نفت، زغال سنگ یا گاز طبیعی دی اکسید کربن یا CO2 تولید می کند، گفته می شود که این گاز گلخانه ای متهم، عامل اصلی گرمایش جهانی است، اما یک ماده خام نیز محسوب می شود، از نظر فنی امکان تبدیل CO2 به ترکیبات کربنی مفید وجود دارد، فرآیندی که نیاز به انرژی، آب، الکترودهای مناسب و کاتالیزورهای ویژه دارد.
CO2 را می توان به صورت الکتروشیمیایی به مونوکسید کربن، فرمت یا متان و همچنین به اتیلن، پروپانول، استات و اتانول تبدیل کرد.
با این حال، فرآیندهای صنعتی باید به گونه ای طراحی شوند که بسیار انتخابی و بسیار کارآمد باشند تا فقط محصولات مورد نظر را تولید کنند و مخلوطی از محصولات را تولید نکنند.
تبدیل مجدد CO2 به سوخت
دکتر متیو مایر، رهبر گروه پژوهشگر جوان هلمهولتز تبدیل الکتروشیمیایی در HZB توضیح داد: با کاهش الکترولیتی CO2 به هیدروکربن های مفید، می توانیم بدون استفاده از منابع فسیلی سوخت های جدیدی تولید کنیم. بنابراین ما CO2 را دوباره به چرخه بازگردانیم، درست مانند بازیافت.
انرژی الکتریکی برای الکترولیز را می توان از طریق انرژی های تجدید پذیر از باد یا خورشید تامین کرد و این فرآیند را پایدار می کند.
از مدرسه می دانیم که الکترولیز را می توان در یک لیوان آب ساده انجام داد و توسعه بیشتر این سلول H است که به شکل حرف H است، با این حال چنین سلول هایی برای استفاده صنعتی مناسب نیستند.
در عوض، الکترولیزهای صنعتی با معماری ساندویچی متشکل از چندین لایه طراحی میشوند: در سمت راست و چپ الکترودهایی قرار دارند که جریان را هدایت میکنند و با کاتالیزورها پوشانده شدهاند، یک لایه انتشار گاز مبتنی بر مس که گاز CO2 را وارد میکند و یک جداسازی غشاء.
الکترولیت (در اینجا در آند عرضه می شود و آنولیت نامیده می شود) از ترکیبات پتاسیم محلول تشکیل شده است و به یون ها اجازه می دهد بین الکترودها حرکت کنند. این غشاء طوری طراحی شده است که به یون های دارای بار منفی اجازه عبور داده و یون های پتاسیم با بار مثبت را مسدود می کند.
مشکل: کریستال های پتاسیم
با این وجود، یونهای پتاسیم از الکترولیت از غشا عبور میکنند و کریستالهای کوچکی را در کاتد تشکیل میدهند که منافذ را مسدود میکند. فلورا هاون، دانشجوی دکترا در تیم متیو مایر، میگوید: «این اتفاق نباید بیفتد. با استفاده از میکروسکوپ الکترونی روبشی و سایر تکنیک های تصویربرداری، دانشمندان توانستند فرآیند تشکیل کریستال در کاتد را با جزئیات مطالعه کنند.
فلورا هاون توضیح داد: با تجزیه و تحلیل پرتو ایکس پراکنده انرژی، ما توانستیم تک تک عناصر را پیدا کنیم و دقیقاً محل تشکیل بلورهای پتاسیم را نشان دهیم.
بررسی ها نشان داد که هرچه الکترولیت حاوی پتاسیم بیشتری باشد، کاتد بیشتر مسدود می شود، اما هیچ راه ساده ای برای حل مشکل وجود ندارد: کاهش غلظت پتاسیم از یک طرف خوب است، اما از طرف دیگر بد است، زیرا تعادل واکنش نیز تغییر می کند: به جای اتیلن مورد نظر، مونوکسید کربن تولید می شود.
الکترولیت کلید حل مشکل
دکتر Gumaa El Nagar، محقق فوق دکترا در این تیم گفت: مهم ترین مشاهدات این است که کاتیون ها هنوز می توانند به غشای تبادل آنیون نفوذ کنند، اما تا حدی که به غلظت الکترولیت بستگی دارد و اینکه با غلظت الکترولیت ما به طور همزمان تنظیم می کنیم که کدام محصولات از CO2 تشکیل می شوند.
دکتر مایر خاطرنشان کرد: در مرحله بعدی، ما میخواهیم از اندازهگیریهای operando و درجا با استفاده از اشعه ایکس استفاده کنیم تا با جزئیات دریابیم که چگونه مهاجرت یون در سلول بر فرآیندهای واکنش شیمیایی تأثیر میگذارد.
در حالی که هنوز نیمی از راه را برای رسیدن به محتوای بهینه CO2 اتمسفر نرسیده ایم، فضایی برای بازیافت وجود دارد. این امر به ویژه در مواردی که گازهای گلخانه ای متراکم از پساب های دیگر پاک می شوند صادق است.
این نکته مثبت این است که به زودی میتوانیم در چرخه کربن سیاره قرار بگیریم.
به عنوان یک هدف بلند مدت که باید اصلی باشد، با این حال در حال حاضر، هیستری تغییرات آب و هوا از نظر سیاسی موضوع غالب است، ترس بسیار مؤثرتر از پیشبینیهای درست و برنامهریزیشده، چشمها را برای رسانهها و تبلیغکنندگان جمع میکند.
این کار فوق العاده مفید بگوییم که نیروگاههای تولید زغالسنگ کل تولید CO2 را دوباره به سوخت بازیافت کردند و این کار استفاده از کربن را قبل از بازگشت به قلمرو گیاهی دو برابر می کند. در واقع سه برابر شدن و بیشتر شدنی بود.
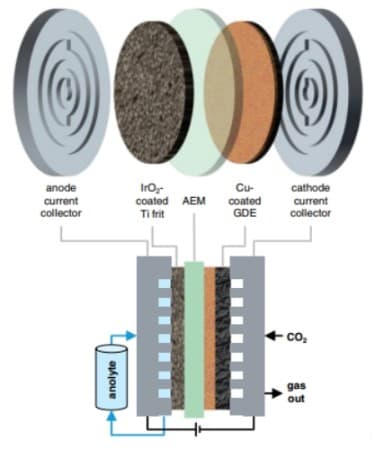
کریستال های پتاسیم در فرآیند جداسازی، غشا را مسدود می کند و دانشمندان به دنبال راه هایی برای کاهش این آلودگی غشا هستند.
لینک سایت مرجع
مالکیت معنوی مجله انرژی (energymag.ir) علامت تجاری ناشر است... سایر علائم تجاری مورد استفاده در این مقاله متعلق به دارندگان علامت تجاری مربوطه می باشد، ناشر وابسته یا مرتبط با دارندگان علامت تجاری نیست و توسط دارندگان علامت تجاری حمایت، تایید یا ایجاد نشده است، مگر اینکه خلاف آن ذکر شده باشد و هیچ ادعایی از سوی ناشر نسبت به حقوق مربوط به علائم تجاری شخص ثالث وجود ندارد.
آیا محتوای این مطلب/مقاله را می پسندید؟
مطالب مرتبط
 تبلیغات در مجله انرژی
تبلیغات در مجله انرژی







